La sincronización y su papel en la formación de patrones biológicos
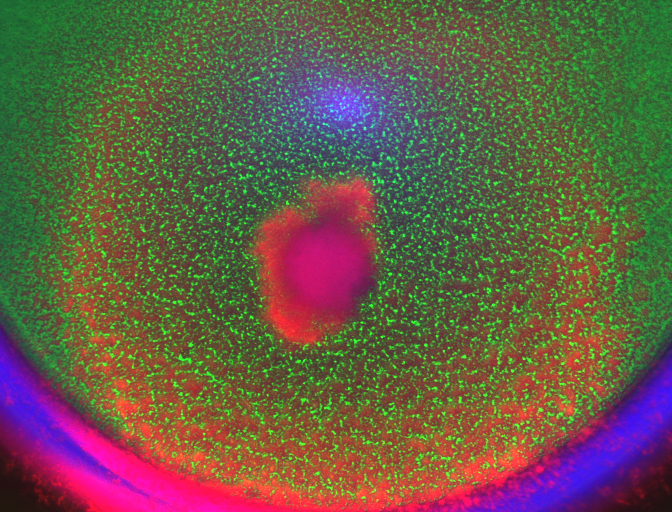
Patrones de anillo se forman en una micro colonia de bacteria modificada. (crédito: Stephen Payne, Pratt School of Engineering, Duke)
Al trabajar con un circuito genético sintético diseñado para hacer que las bacterias crezcan en un patrón predecible de anillos, los científicos de la Universidad Duke han dado a conocer un subestimado miembro que contribuye a la formación natural de patrones: el tiempo.
En una serie de experimentos publicados en octubre 8, 2013, en la revista Molecular Systems Biology, Lingchong You y sus colegas demostraron que los circuitos de genes manufacturados funcionan como un mecanismo de tiempo, lo que provocó un patrón de crecimiento en forma de anillos que se adapta al tamaño de su entorno.
El inesperado resultado da una posible explicación sobre la manera en que órganos como el corazón y los pulmones saben cuándo dejar de crecer y contradice teorías establecidas, una de las cuales se remonta a Alan Turing, pionero de la computación. El hallazgo también establece una base de bacterias modeladas como una estructura biológica para nuevos materiales, tales como películas metálicas, que tienen aplicaciones potenciales en energía.
Morfógenos de Turing
Las ideas de Turing han guiado las teorías de formación de patrones en biología por décadas. Turing imaginó que los patrones biológicos surgían de la interacción de sustancias químicas que denominó “morfógenos” que iniciaban y dirigían los patrones al activar su interruptor de encendido o apagado, dependiendo de su concentración en un lugar específico. En un tratado teórico publicado en 1952, Turing usó matemáticas para demostrar cómo los morfógenos podrían moverse en el espacio, revelando así patrones que imitan a los observados en pieles de animales y formas de hojas.
Pero al igual que un mito persistente, las teorías pueden también arraigarse. You y sus colegas quedaron perplejos cuando un circuito genético sintético que construyeron para poner a prueba el modelo de Turing no creó el patrón de crecimiento que esperaban.
Por medio del uso de técnicas de biología molecular, You y sus colegas habían programado la bacteria común de laboratorio conocida como E. coli para producir dos moléculas. Una servía como interruptor de “encendido” para extenderse por la creciente colonia. La otra, el interruptor de “apagado” sería desencadenado por una creciente concentración de la señal de “encendido”.
Los investigadores también diseñaron estas bacterias para generar colores fluorescentes y ver así la forma de los patrones. Pero a medida que las colonias crecieron, los patrones no se comportaron como se suponía. Eran mucho más pequeños que lo esperado por el equipo de investigación basados en la rapidez que debía difundirse la señal de “encendido”.
Una señal de sincronización
Para resolver este misterio, los científicos añadieron una alta concentración de señal de “encendido” en la cámara de crecimiento, inundando las bacterias con esta señal. Las bacterias formaron el mismo patrón distintivo de anillos durante el mismo tiempo, lo que demostraba que no respondían a los cambios en la concentración de la señal de “encendido”.
En su lugar, los investigadores razonaron que la señal de “encendido” servía como una señal de sincronización. El equipo de investigación creó un modelo matemático del mecanismo de sincronización y predijo la manera en que las células responderían a los cambios en tamaño de su cámara de crecimiento.
“Al servir como una señal de sincronización, el morfógeno de la señal ‘encendido’ permite que el sistema detecte y responda al tamaño de su ambiente”, dijo You. “Mientras mayor el área, más tiempo tomará el morfógeno para lograr una concentración lo suficientemente alta para provocar la formación de patrones. Como tal, un área más grande dará lugar a un patrón de anillo más grande” .
Experimentos posteriores confirmaron el modelo, y proporcionó un ejemplo simple de cómo los órganos en crecimiento pueden ser capaces de detectar el tamaño de su entorno –y detectar así el momento de dejar de crecer– resolviendo potencialmente un misterio persistente en biología del desarrollo.
You y sus colegas planean ya utilizar el circuito genético artificial para crear patrones biológicos más complejos, tanto para explorar más a fondo los principios generales de formación de patrones, así como para utilizarse de estructura para la fabricación de nuevos materiales, tales como películas delgadas de metal para aplicaciones de energía.
Más información aquí.


Comentarios